 风湿消息
风湿消息
漫话风湿系列连载(三)“万用细胞”点亮重生希望——干细胞移植
(一)什么是干细胞
在了解干细胞为什么能作为“万用细胞”点亮风湿病患者重生希望之前,我们先要对干细胞有一定的认识。干细胞是人体的起源细胞,具有自我更新和多向分化潜能。所谓自我更新,即细胞通过有丝分裂产生的两个子代细胞仍具有分裂前的增殖和发育潜力。所谓多相分化,即它们具有相同的向多种细胞发育的潜力,只是由于单个细胞所处的微环境不同,受控于不同的调节系统才发育成不同的后代。干细胞由受精卵发育分化而来,最初形成原始胚胎干细胞,然后分化增殖为能形成人体各种组织的全能干细胞,并逐步分化为多能干细胞,最终分化为具有特定功能的组织专能干细胞。由于干细胞具有这种生物学特性,故被称为“万用细胞”。
在人类造血组织中,存在有三种干细胞,分别为造血干细胞(HSC)、血管干细胞和间充质干细胞(MSC)(间质干细胞、基质细胞)。在本章节中主要讲述造血干细胞和间充质干细胞。HSC是造血系统细胞的鼻祖,它具有向各种髓细胞和淋巴细胞发育的潜能,同时也具有一定的自我更新能力,可通过移植重建受损的造血系统和免疫系统。MSC最早是由俄罗斯学者于1976年报道,并定义为构成成人骨髓微环境的一种具有粘附性的、成纤维细胞样的细胞群,约占成人骨髓细胞的0.001%-0.01%。这群细胞作为干细胞的一种,也具有自我更新和多向分化能力。
我们通常所说的干细胞移植一般指的是造血干细胞移植(HSCT)和间充质干细胞移植(MSCT)。这两种干细胞移植在治疗风湿病方面都有其独到之处,在部分患者身上有着药物无法比拟的效果而为风湿病患者点亮重生希望。下面我们就这两种干细胞移植的相关知识作一介绍。
(二)HSCT
1.HSCT治疗风湿病的演变
1977年,欧洲有4例类风湿关节炎(RA)患者在使用金制剂后引起重型再生障碍性贫血(SAA),这4例患者接受异基因骨髓HSCT治疗后,人们意外而惊喜地发现在SAA得到缓解的同时,RA也得到不同程度的缓解。这就是HSCT治疗风湿病的最早来源。1993年,意大利圣马丁医院骨髓移植中心的Marmont在Lupus杂志上提出HSCT治疗SLE的设想。1995年,欧洲抗风湿病联盟(EULAR)和欧洲骨髓/血液移植协作组(EBMT)提出了HSCT治疗自身免疫病(AD)的初步方案。1996 年9 月,他们在瑞士巴塞尔召开了第一届国际HSCT治疗AD专题研讨会,对原方案进行了修订统一,并开始多中心研究HSCT治疗重症AD。1997年,英国谢菲尔德大学Snowden等在英国血液学杂志上发表文章,详尽评估了HSCT治疗AD。同年,Marmont在国际上首次用自体骨髓HSCT治疗了一例系统性红斑狼疮(SLE)患者,该患者在造血重建后狼疮获得临床缓解。几乎同时,美国西北大学Burt也用HSCT治疗了美国首例SLE患者。此后,世界各国包括我国陆续开展了该领域的研究。目前,国际上有多项HSCT治疗AD的前瞻性临床研究正在进行中,全世界已有超过1000例难治性AD患者接受了HSCT。在基础研究方面, HSCT治疗风湿病的机制、移植后免疫重建是目前研究的热点。这些临床和基础研究不仅可能为HSCT治疗风湿病提供更加客观、详实的依据,而且对于探讨HSCT治疗风湿病的机制、移植后复发的机制甚至风湿病本身的发病机制均具有重大意义。
2.HSCT的相关知识
(1)根据采集途径不同,HSCT可分为3种类型:骨髓移植(BMT)、外周血干细胞移植(PBSCT)和脐带血移植(CBT)。
BMT就是将正常的骨髓移植到患者不正常或失去造血功能的骨髓里,恢复患者的造血功能,是经典的移植方法。确定供者后,患者需要进行大剂量放、化疗来产生足够的免疫抑制以防残存的宿主免疫活性细胞破坏移植物,并且杀伤残存的异常细胞,为新植入的骨髓提供适当的生长空间。
PBSCT是使用造血生长因子等方法将造血干细胞从骨髓中动员至外周血,再通过血细胞分离机从循环血中收集造血干细胞,与骨髓移植相比,具有采集方便、供者不需全麻、采集安全、移植后造血恢复快等优点。
CBT是将胎儿脐带血中的HSC移植给患者。胎儿脐带血中这些大量的HSC,免疫原性较弱,且与骨髓干细胞相比,具有更高的增殖潜能,多用于儿童患者。
(2)根据HSC来源不同,HSCT又可分为异基因HSCT(allo-HSCT)、同基因HSCT(syn-HSCT)和自体HSCT(auto-HSCT)。
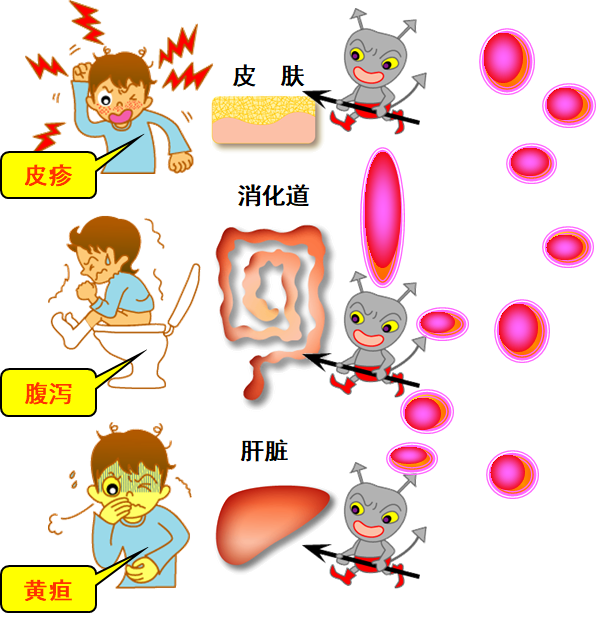
allo-HSCT的主要优势是移植物无异常细胞污染、具有移植物抗肿瘤细胞效应或抗自身免疫效应;缺点是难以找到HLA相合的供者和可能发生移植物抗宿主病(GVHD)。GVHD是allo-BMT的严重而常见的并发症,表现为皮肤、胃肠道及肝脏症状(如图1)。发生于移植后1~3个月的为急性GVHD,慢性GVHD则发生于移植后100天或更长时间。因为GVHD发生率与受者年龄呈正相关,这使allo-HSCT对老年患者的应用受到限制。
图1 GVHD常见表现
syn-HSCT是指受者与供者基因完全相同的HSCT。在人类,仅少数的同卵双胎孪生兄弟或姐妹间的移植是此种移植,其优势为疗效高,无GVHD发生。但这种移植机会非常少,限制了使用。
auto-BMT为大剂量预处理后应用患者自身骨髓重建造血功能。其最大的优势是无GVHD发生,干细胞来源容易。而缺点是自体HSC里面可能有异常细胞;缺乏移植物抗肿瘤或抗自身免疫效应,接受多次化疗的患者骨髓HSC含量可能较少。因此,难以收集到足够供移植的HSC。
无论哪种HSCT,其基本过程和原理都是用放/化疗对患者进行清髓性或非清髓性预处理后,植入HSC,从而达到造血重建及免疫重建的过程(如图2)。
3.HSCT治疗风湿病的方法选择和评价
(1)allo-HSCT
从理论上讲,异基因移植可能更为有效,这是因为:可破坏清除所有自身免疫T淋巴细胞克隆和记忆细胞;回输的干细胞源于健康供者,不会混入患者自身的自身反应性免疫细胞;移植物可产生移植物抗自身免疫效应。但allo-HSCT在血液病中死亡率和致残率达15~30%,远高于auto-HSCT,并且在移植后可出现GVHD。因此,目前allo-HSCT对于风湿病并非首选。
(2)大剂量淋巴细胞清除治疗后不进行干细胞移植
Petri等报道14例SLE,单用环磷酰胺(CTX)50mg/kg·d,连用4天,辅以粒细胞集落刺激因子(G-CSF)促进造血恢复。结果5例完全缓解,6例部分缓解。提示在这部分患者中起主要作用的可能是CTX预处理,而非异基因骨髓提供新的干细胞来源及移植物抗自身免疫效应。不过从临床疗效看,虽然其耐受性尚可,但造血恢复迟于auto-HSCT,CTX可能起了大剂量免疫抑制作用,复发率较高,总体疗效不及auto-HSCT。
(3)auto-HSCT
与前两种策略相比较,auto-HSCT显得最为安全,对于风湿病是优先选择的移植方案。该方案的优点是不需要寻找供者、安全性高、移植后患者生活质量高、治疗费用低;但其最大的缺点是疾病复发率高。又因为动员干细胞时多数应用化疗药物,相当于进行了两次化疗,其临床疗效优于单纯大剂量化疗。而应用大剂量CTX这类非清髓性化疗药物时,回输干细胞可缩短造血重建时间,从而降低治疗风险。
4.HSCT治疗风湿病的方案
1995年在西雅图和1996年在巴塞尔风湿病学和骨髓移植学专家共同研讨HSCT治疗AD的方案,出于安全考虑,认为首选auto-HSCT,尤其是auto-PBSCT。
auto-PBSCT治疗风湿病的过程一般包括干细胞动员、采集、冻存、预处理和干细胞回输。目前动员HSC的方法有3种:单纯化疗动员;化疗+G-CSF动员;单纯G-CSF动员。对于风湿病,干细胞动员方案多选用CTX化疗加G-CSF。最常用的预处理方案有CTX、CTX/抗胸腺细胞免疫球蛋白(ATG)、CTX/全身照射(TBI)、CTX/马利兰、BEAM等。
5.HSCT治疗风湿病的适应症
(1)系统性红斑狼疮(SLE)
对SLE目前还无最佳的入选标准,多数学者同意将预计预后不良的病例纳入。综合各家的标准,至少有下列一项表现者可考虑进行HSCT治疗:出现癫痫或精神症状;肺部受累至少有以下一项:肺出血、浸润而无感染并存,最近6个月内用力肺活量降低大于15%,肺动脉高压;难治性溶血性贫血,网织红细胞计数大于3%,血红蛋白低于
(2)系统性硬化(SSc)
SSc的入选标准较明确,即进展性弥漫型SSc。具体标准为:病程小于3年;弥漫性皮肤损害以及改良Rodnan积分(mRSS)大于16分;同时合并下列至少一项内脏损害:肺部有活动性肺泡炎或用力肺活量小于80%;肾脏累及出现蛋白尿和血清肌酐水平升高;心脏受累出现心律失常、心脏扩大或心包积液;也有一些研究者将伴有进行性肺动脉高压的CREST综合征也纳入。
(3)类风湿关节炎(RA)
综合各家标准,必须符合下列情况:病情诊断明确;对常规治疗无效。近期的标准则要求先进行抗肿瘤坏死因子治疗,如无效方可考虑移植;有预后不良因素存在,如类风湿因子持续阳性、关节破坏侵蚀、有关节外表现等。
(4)幼年特发性关节炎(JIA)
与其他风湿病一样,JIA的入选标准应是预后不良者,如存在持续发热、糖皮质激素依赖,并且包括抗肿瘤坏死因子治疗无效者。
6.HSCT治疗风湿病的国内外现状
根据IBMTR和ABMTR统计中心提供的数据,到2004年,EBMT和IBMTR/ABMTR(Autologous
Blood and Marrow Transplant Registry)登记治疗的患者有800例,其中风湿病有416例。移植的病种病例数由多到少为SLE、RA、SSc、JIA(如表1)。至2006年,EBMT登记的患者中,SSc增加至126例,SLE增加至79例,RA增加至76例,JIA增加至62例。下面就几种常见风湿病谈谈HSCT的国内外现状。
表1 至2013年9月EBMT登记的HSCT治疗风湿病病种及例数
自体HSCT | 异体HSCT | |
多发性硬化 | 544 | 4 |
系统性红斑狼疮 | 99 | 6 |
系统性硬化 | 330 | 1 |
关节炎 | 163 | 11 |
克隆病 | 109 | 3 |
血管炎 | 50 | 8 |
免疫相关血细胞减少 | 42 | 43 |
神经病变 | 50 | 4 |
其他 | 84 | 18 |
(1)SLE
尽管HSCT治疗SLE已有16年的历史,但是仍缺乏多中心前瞻性的临床研究结果,大宗的临床研究报告也较少。至今较有代表性的研究报告分别来自美国西北大学和EBMT/ EULAR登记处。西北大学报道了自体HSCT对50例SLE患者的治疗结果,这些患者均为对标准免疫抑制治疗无效、存在脏器功能障碍或危及生命的内脏受累情况。移植后5年无病生存率为50%,移植相关死亡率为4%,80%的患者在移植后SLEDAI评分、血清抗核抗体、抗ds-DNA抗体、补体、一氧化碳肺弥散量等指标均有明显改善。严重感染仍是SLE患者HSCT后的主要风险,感染多发生在移植后100天内,细菌、真菌及病毒均为常见病原体。
南京鼓楼医院1998年在亚洲首先开展自体骨髓移植治疗难治性SLE取得成功。后国内有多家医院将HSCT治疗SLE应用于临床。南方医院用Auto-PBSCT治疗12例SLE患者,6个月后患者血清中抗核抗体、抗ds-DNA抗体、抗RNP抗体、抗Sm抗体的含量恢复正常。华中科技大学附属同济医院对8例Auto-PBSCT治疗的SLE患者的风险进行分析,结果8例均出现移植后感染,真菌、巨细胞病毒、带状疱疹病毒感染各1例,5例出现心血管并发症,表现为急性左心衰竭、心房纤颤和频发室性早搏,未出现严重的肝、肾功能损害。
(2)RA
RA波及世界约1%的人口,难治性患者是HSCT的适应症。目前规模最大的报道是EBMT/ABMTR所登记的76例RA患者,其中73例难治性RA患者接受了Auto-PBSCT49例(67%)患者达到ACR50%反应,生活质量显著提高。
北京协和医院在国内首次对1例RA患者进行Auto-PBSCT治疗,移植后随访12个月,患者关节肿痛完全消失,生活质量明显改善,血沉、C-反应蛋白降至正常,类风湿因子转阴。
(3)SSc
近年来,国外很多I期、II期临床研究证实,Auto-HSCT使大多数SSc患者皮肤病变得到改善,肺部病变得到稳定,但是,与预处理和移植相关的死亡率高达17%。至2002年8月,EBMT/EULAR登记来自9个国家22个中心的57例严重SSc患者,结果14%的患者死于本身疾病进展,5年存活率达72%,存活的50例患者移植后至少随访6个月,92%的患者得到了部分或完全缓解。
(4)JIA
9个儿科骨髓移植机构和EBMT数据库共登记了52例JIA患儿,分析了其中34例难治性患儿。25例接受了BMT,另9例在用CTX和G-CSF动员后接受了PBSCT。随访6~60个月,17例(50%)达到ACR70%反应,生活质量得到很大改善,但关节活动受限无改善,6周内血沉、C反应蛋白和血红蛋白恢复接近正常。其中1例感染水痘、带状疱疹,另1例出现扁桃体炎。4例(12%)对HSCT无效,4例(12%)患儿死于骨髓抑制期感染。
7.HSCT治疗风湿病的机制
风湿病是一类异质性很强的疾病,在多种易感背景和环境因素启动下,对自身抗原产生病理性反应的过程。其发病机制虽不明确,但T、B淋巴细胞功能的异常在发病中的作用基本公认,淋巴细胞的功能异常导致多种细胞因子及多种自身抗体产生,进一步损伤机体组织器官。关于HSCT治疗自身免疫病的机制有很多假说,如“重建免疫系统”(reseting the immune system)、“逆转免疫时相”(truning
back the immunological clock)、“减轻炎症负荷”(debulking of inflammatory load)。迄今为止,机制不完全清楚,可能包括移植预处理方案中大剂量放化疗的免疫清除;T、B淋巴细胞再生过程中诱导免疫耐受;免疫重建过程中达到新的免疫平衡;allo-HSCT的GVA效应;混合嵌合体(MC)诱导免疫耐受。
8.HSCT治疗风湿病的利弊评价
从目前全球大规模的HSCT治疗风湿病的结果来看,HSCT 对风湿病患者有较好的耐受性并且大多数患者可获得缓解。遗憾的是, 移植后疾病的复发很常见,但有些复发的患者又重新获得了对既往无效药物的敏感性。而且,异体移植相关的并发症如GVHD、感染也是我们面临的一大难题。由于HSCT治疗AD时间不长,例数和随访时间有限,目前尚不能得出HSCT可使风湿病获得长期缓解的结论,更谈不上根治或治愈。这就要求我们寻找比HSCT更有潜力、风险更小的方法。
(三)MSCT治疗风湿病潜力巨大
1.MSC独特的生物学特性
1976年,俄罗斯Friedenstein首先发现在塑料培养皿中培养的贴壁骨髓单个核细胞在一定条件下可分化为多种中胚层来源的间质细胞,自此,这群单个核细胞被命名为MSC。这是一类来源于基质组织的多能祖细胞,最初为人类所认识是因为它有支持造血及组织再生的功能。它的低/无免疫原性、多向分化能力、归巢及组织修复能力使之在组织工程及细胞治疗方面备受关注。MSC具有易纯化、体外扩增迅速、可长期传代的特点,可从多种组织如骨髓、脐带、脐带血、脂肪等组织中分离培养。脐带MSC由于其细胞更原始、来源更广泛而成为目前MSC治疗中的主力军。
2.MSC可发挥长期的免疫调节作用
MSC的免疫调节功能为学术界广泛关注,但这一免疫调节作用的机制还不明确。MSC的免疫学特性研究大多建立在体外细胞培养基础上,大量的体外细胞培养试验证明它具有诱导免疫耐受和免疫调节的特性。而且,MSC在分化成其他细胞类型时仍保留其免疫调节作用,这就意味着移植的MSC可发挥长期的免疫调节作用。此外,MSC的无或低免疫原性,不需要MHC配型,非常适合于细胞治疗。MSC可诱导宿主免疫耐受,即使输入异种MSC也不产生排斥反应。所以,MSC在风湿病治疗中前景广泛。
3. AD是一种干细胞病
我们研究发现:SLE患者骨髓MSC较正常人骨髓MSC体外生长迟缓,不能长期传代,有早衰现象,细胞骨架排列紊乱,成骨、成脂肪分化功能异常,白介素(IL)-6、IL-7体外分泌明显低于正常。因此,我们提出“SLE不仅是造血干细胞病,而且是间充质干细胞病,异体MSC移植治疗SLE更合适”的新观点MSC本身基因表达的异常是先天还是后天的尚不清楚。另外;是MSC本身的异常参与了发病还是疾病导致了MSC的异常也不清楚。
4. MSC移植治疗SLE模型
我们的研究结果显示,SLE模型鼠(MRL/lpr和NZB/NZW F1)在接受MSCT后,生存率明显提高,尿蛋白下降,抗核抗体和抗双链DNA抗体下降,血清肌酐、尿素氮水平下降,肾脏病理变化和免疫复合物沉积明显减轻, 且未发生排斥反应。由此可见 MSCT治疗SLE安全、有效。
5. MSC成为风湿病患者的新希望
(1)MSCT治疗SLE
经南京大学医学院附属鼓楼医院伦理委员会批准,2007年3月我们在国际上首先尝试用异基因骨髓MSCT治疗难治性SLE患者,至今已完成近300余例,部分结果发表于Arthritis & Rheumatism、Ann Rheum Dis、Nat Rev Rheumatology、Cell Transplantation等杂志上。2012年,对异基因MSCT治疗的87例难治性SLE患者随访4年的结果进行了报道,结果显示4年生存率为94%(82/87),1年、2年、3年、4年时的完全临床缓解率分别为28%、31%、42%和50%,复发率分别为12%、18%、17%和17%,总复发率为23%。总的完全和部分缓解率达60%,移植后患者的SLEDAI评分显著下降,血清自身抗体、血白蛋白、血清补体等得到明显改善。5例(6%)患者在随访的4年中死亡,无移植相关死亡。弥漫性肺泡出血为SLE的一种严重并发症,死亡率达50%。我们用MSCs移植成功抢救了4例这样的患者,这些患者的病情均得到了明显改善。
(2)MSCT治疗RA
2012年,我们报道了MSCT治疗的4例生物制剂治疗无效的难治性RA患者,其中3例在移植后1个月和6个月时血沉、DAS28和疼痛评分均明显下降。2例患者在6个月时达到EULAR中度反应,但在第7个月和第23个月病情复发。未发现移植不良反应。
(3)MSCT治疗多发性肌炎/皮肌炎(DM/PM)
2011年,我们对10例接受MSCT的DM/PM患者进行了报道,结果显示所有患者的肌酸激酶、疾病总体评分、间质性肺炎都有所改善,1例长期皮肤溃疡的患者MSCT后溃疡愈合。
(4)MSCT治疗干燥综合征(SS)
至2012年,我们用MSCT治疗了24例SS患者,所有患者都无不良反应,在2周到6个月后干燥的症状均得到了改善,平均SSDAI评分分别从移植前的5.63±1.44降低到4.58±1.67(2周)、4.33±1.79(1个月)、4.08±1.44(3个月)、3.46±1.18(6个月)以及3.08±1.21(1年)。这些患者的疾病总体评分也得到了明显降低,3个月、6个月、1年时分别有37.5%、58.3%、75%的患者疾病总体评分下降超过30%。移植后11例患者的唾液流率明显增加。4例血小板减少的患者在移植后2周血小板均明显上升;3例难治性贫血的患者在移植后血红蛋白也明显上升;7例SS相关的自身免疫性肝损患者,肝功能得到改善;3例神经系统受累的患者在移植后无明显改善。
(5)MSCT治疗SSc
2013年,我们对5例接受MSCT的SSc患者进行报道,这些患者的改良Rodnan皮肤评分和健康问卷疾病活动指数均得到了明显改善,血清抗核抗体水平在移植后12个月时明显下降。
(6)MSCT治疗炎症性肠病(IBD)
2011年,我们报道了MSCT对7例IBD患者的疗效,其中4例为克罗恩病,3例为溃疡性结肠炎,中位随访时间19个月。结果所有患者腹泻和腹痛都逐渐减轻,疾病活动指数明显下降。移植后3个月时5例患者达到缓解,2例患者持续缓解到24个月,2例患者在第6个月和第7个月复发。4个月时,所有患者的结肠的镜下表现明显好转,3例患者的结肠组织学得到改善。3例患者的糖皮质激素逐渐减量。
(7)MSCT治疗多发性硬化(MS)
我们曾用MSCT治疗了1例难治性MS患者,患者治疗半年无效,全身麻木瘫痪,MSCT后 3天,患者下肢肌力开始恢复;移植后第 6天,躯体麻木感开始减轻;移植后第9天,肌力进一步回复,患者可在帮助下坐起;移植后1个月,患者可在搀扶下行走
6.MSCT治疗风湿病评价
MSCT现已成为风湿病治疗领域里的一大热点研究方向。MSC的优点在于能重建免疫、支持造血、组织修复,更重要的是其具有诱导免疫耐受及免疫调节作用且不具有免疫原性,即使输入异基因MSC,宿主也不会发生排斥反应,这就可以解决在异基因造血干细胞移植中 HLA不相合的问题。此外,MSC来源广、费用低、不需要大剂量化疗预处理、不需要层流病房、无并发症等优点,MSCT治疗风湿病前景广阔,随着大规模多中心临床研究的开展,相信不久的将来MSCT治疗AD完全有可能和生物制剂相媲美,对风湿病的治疗带来革命性的挑战。
(本章作者:孙凌云)
版权所有 © 北京大学人民医院风湿免疫研究所
技术支持:优河马